

12/10/2023


Làm sao để có câu trả lời hay nhất?
- Luôn có GIẢI THÍCH các bước giải
- Không copy câu trả lời của Timi
- Không sao chép trên mạng
- Không spam câu trả lời để nhận điểm
- Spam sẽ bị khóa tài khoản



12/10/2023

12/10/2023

a)
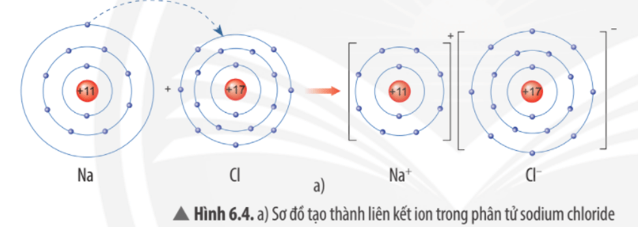
Khi nguyên tử sodium (Na) kết hợp với nguyên tử chlorine (Cl), nguyên tử Na nhường 1 electron tạo thành ion dương, kí hiệu là Na+, đồng thời nguyên tử Cl nhận 1 electron từ nguyên tử Na tạo thành ion âm, kí hiệu Cl-. Ion Na+ và Cl- hút nhau tạo phân tử sodium chloride (NaCl).
b)
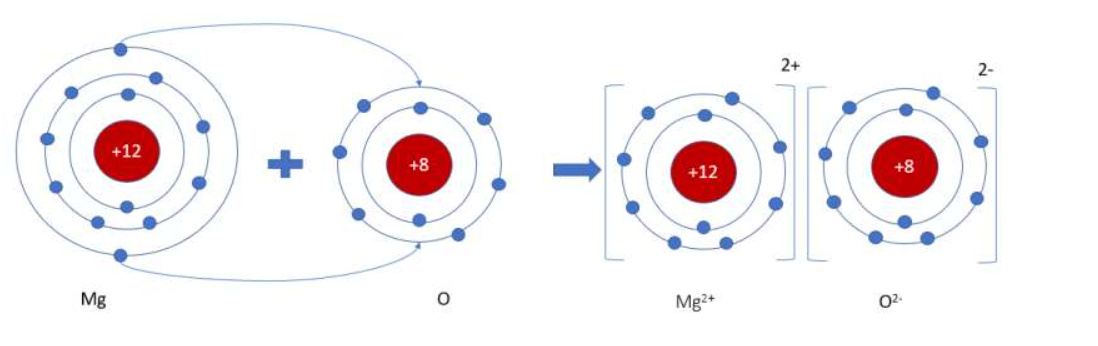
- Nguyên tử Mg (có số hiệu nguyên tử = 12) nhường 2 electron cho O, tạo thành ion Mg2+
- Nguyên tử O (có số hiệu nguyên tử = 8) nhận 2 electron từ Mg, tạo thành ion O2-
=> Ion dương Mg2+ và ion âm O2- mang điện tích trái dấu nên hút nhau, tạo thành liên kết ion

12/10/2023
- Natri clorua (NaCl): Trong phân tử NaCl, nguyên tử natri (Na) mất đi một electron để trở thành ion natri dương (Na+), trong khi nguyên tử clo (Cl) nhận electron này để trở thành ion clo âm (Cl-). Hai ion này được liên kết với nhau thông qua lực tương tác điện từ, tạo thành một liên kết ion.
- Canxi florua (CaF2): Trong phân tử CaF2, nguyên tử canxi (Ca) mất hai electron để trở thành ion canxi dương (Ca2+), trong khi hai nguyên tử fluor (F) nhận các electron này để trở thành ion fluor âm (F-). Hai ion canxi và bốn ion fluor tạo thành một cấu trúc tinh thể, trong đó lực tương tác điện từ giữ chúng lại với nhau.
- Nhôm oxit (Al2O3): Trong phân tử Al2O3, hai nguyên tử nhôm (Al) mất ba electron để trở thành ion nhôm dương (Al3+), trong khi ba nguyên tử oxi (O) nhận các electron này để trở thành ion oxi âm (O2-). Ba ion nhôm và sáu ion oxi tạo thành một cấu trúc tinh thể, trong đó lực tương tác điện từ giữ chúng lại với nhau.
Lưu ý rằng đây chỉ là một mô tả tổng quát về quá trình liên kết ion trong các hợp chất này. Sự liên kết ion xảy ra khi có sự trao đổi electron giữa các nguyên tử để tạo ra các ion trái dấu, và lực tương tác điện từ giữa các ion này làm cho chúng liên kết với nhau.
Đăng nhập hoặc Tạo tài khoản miễn phí!

 Điện thoại: 1900636019
Điện thoại: 1900636019
 Email: info@fqa.vn
Email: info@fqa.vn
LIÊN KẾT
- Hỏi đáp bài tập
- Giải bài tập SGK
- Cẩm nang
- Đề ôn luyện
- Điều khoản & chính sách
- Sitemap
- Liên hệ
- Đánh giá và góp ý
FQA.vn Nền tảng kết nối cộng đồng hỗ trợ giải bài tập học sinh trong khối K12. Sản phẩm được phát triển bởi CÔNG TY TNHH CÔNG NGHỆ GIA ĐÌNH (FTECH CO., LTD)
Copyright © 2025 fqa.vn All Rights Reserved












