Tất cả
Hỏi bài tập Toán Học
Vật Lý
Hóa Học
Tiếng Anh
Ngữ Văn
Hỏi đời sống Tâm lý cảm xúc
Tình cảm
Gia đình bạn bè
Cơ thể & Dậy thì
Giải trí
Mạng xã hội
Định hướng cuộc sống
Hỏi đáp ẩn danh
Trình bày cấu trúc electron bền vững của khí hiếm.
 1
1
-
Câu trả lời phải chính xác, đầy đủ dựa trên kiến thức xác thực:
- ✔ Đối với câu hỏi trắc nghiệm: Đưa đáp án lựa chọn + giải thích lý do chọn đáp án.
- ✔ Đối với câu hỏi tự luận: Đưa lời giải và đáp án cho câu hỏi.
- ✔ Đối với câu hỏi trả lời ngắn: Đưa ra đáp án + giải thích lý do.
- ✔ Chấp nhận sử dụng ảnh do thành viên viết tay, ảnh cần rõ nét, không bị mờ, vỡ ảnh.
- Sử dụng ngôn ngữ rõ ràng, dễ hiểu.
- Tránh đưa ra các ý kiến cá nhân mang tính chất chủ quan.
- Nếu sử dụng thông tin từ nguồn khác, phải trích dẫn nguồn đầy đủ và chính xác.
- Tuyệt đối không được sao chép các thông tin từ các trang khác, từ AI hoặc chatGPT.



20/04/2024
 0
0
20/04/2024
- Các nguyên tố khí hiếm thuộc nhóm VIIIA của bảng tuần hoàn.
⇒ Cấu hình electron lớp ngoài cùng dạng: ns2np6 trừ He là 1s2.
- Cấu hình electron của 1 số khí hiếm hay gặp:
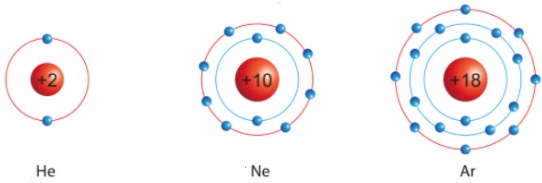
+ Heli (He): 1s2.
+ Neon (Ne): 1s22s22p6.
+ Argon (Ar): 1s22s22p63s23p6 viết gọn là [Ne]3s23p6.
+ Kripton (Kr): 1s22s22p63s23p63d104s24p6 viết gọn là [Ar]3d104s24p6
 0
0
20/04/2024
Cấu trúc electron bền vững của khí hiếm được xác định bởi cấu trúc electron của nguyên tử của khí đó. Một số khí hiếm như Helium (He), Neon (Ne), Argon (Ar), Krypton (Kr), Xenon (Xe) và Radon (Rn) có cấu trúc electron bền vững do chúng đều thuộc nhóm 18 (hoặc còn gọi là nhóm 0 hoặc nhóm khí hiếm) trong bảng tuần hoàn nguyên tố.
Cấu trúc electron của các nguyên tử trong nhóm 18 là bền vững vì chúng đều có số electron bằng với số proton trong hạt nhân, tạo ra cấu trúc electron hoàn chỉnh và không cần phải chia sẻ hoặc nhận thêm electron để đạt được cấu trúc electron bền vững. Điều này làm cho các khí hiếm có tính ổn định và ít tương tác với các nguyên tử khác, làm cho chúng trở thành các khí không phản ứng nhiều với các yếu tố khác trong môi trường.
 1
1
Nếu bạn muốn hỏi bài tập
Các câu hỏi của bạn luôn được giải đáp dưới 10 phút
CÂU HỎI LIÊN QUAN
Top thành viên trả lời



