Tất cả
Hỏi bài tập Toán Học
Vật Lý
Hóa Học
Tiếng Anh
Ngữ Văn
Hỏi đời sống Tâm lý cảm xúc
Tình cảm
Gia đình bạn bè
Cơ thể & Dậy thì
Giải trí
Mạng xã hội
Định hướng cuộc sống
Hỏi đáp ẩn danh
15/10/2024
Cho các phân tử sau: CH4, C2H4, C2H2, HCl, CCl4, CF4, PCl3?
a. Dựa vào các thuyết liên kết hóa học hãy giải thích sự hình thành liên kết và cấu dạng hình học của phân tử đó?
b. Hãy cho biết các nguyê...
 0
0
-
Câu trả lời phải chính xác, đầy đủ dựa trên kiến thức xác thực:
- ✔ Đối với câu hỏi trắc nghiệm: Đưa đáp án lựa chọn + giải thích lý do chọn đáp án.
- ✔ Đối với câu hỏi tự luận: Đưa lời giải và đáp án cho câu hỏi.
- ✔ Đối với câu hỏi trả lời ngắn: Đưa ra đáp án + giải thích lý do.
- ✔ Chấp nhận sử dụng ảnh do thành viên viết tay, ảnh cần rõ nét, không bị mờ, vỡ ảnh.
- Sử dụng ngôn ngữ rõ ràng, dễ hiểu.
- Tránh đưa ra các ý kiến cá nhân mang tính chất chủ quan.
- Nếu sử dụng thông tin từ nguồn khác, phải trích dẫn nguồn đầy đủ và chính xác.
- Tuyệt đối không được sao chép các thông tin từ các trang khác, từ AI hoặc chatGPT.



15/10/2024
 0
0
15/10/2024
Công thức Lewis của CH4 là
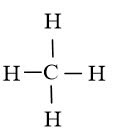
Từ công thức Lewis của CH4 ta xác định được phân tử này có dạng tứ diện theo mô hình VSEPR.
Cấu hình electron của C (Z = 6) là 1s22s22p2
1 AO 2s tổ hợp với 3 AO 2p tạo 4 AO lai hóa sp3
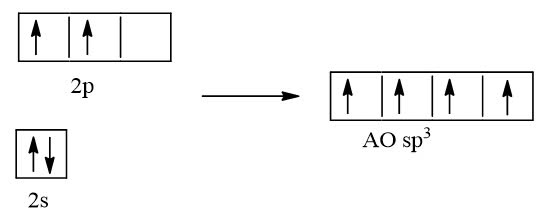
4 AO lai hóa sp3 của nguyên tử C xen phủ với 4 AO s của nguyên tử H tạo thành 4 liên kết σ hướng về 4 đỉnh của một tứ diện đều.
 0
0
15/10/2024
1. **CH4 (Metan)**:
- Nguyên tử carbon (C) có 4 electron ở lớp ngoài cùng và cần 4 electron để đạt cấu hình bền. Do đó, nó hình thành 4 liên kết đơn với 4 nguyên tử hydro (H) thông qua liên kết cộng hóa trị. Cấu dạng hình học của CH4 là hình tứ diện, với góc liên kết khoảng 109.5°.
2. **C2H4 (Etilen)**:
- Mỗi nguyên tử carbon trong C2H4 có 4 electron ở lớp ngoài cùng. Hai nguyên tử carbon hình thành một liên kết đôi (1 liên kết sigma và 1 liên kết pi) và mỗi carbon còn lại hình thành 2 liên kết đơn với 2 nguyên tử hydro. Cấu dạng hình học của C2H4 là phẳng, với góc liên kết khoảng 120°.
3. **C2H2 (Acetilen)**:
- Trong C2H2, hai nguyên tử carbon hình thành một liên kết ba (2 liên kết pi và 1 liên kết sigma) và mỗi carbon còn lại hình thành 1 liên kết đơn với 1 nguyên tử hydro. Cấu dạng hình học của C2H2 là tuyến tính, với góc liên kết là 180°.
4. **HCl (Axit clohidric)**:
- HCl là một phân tử đơn giản với một liên kết đơn giữa nguyên tử hydro và nguyên tử clo. Cấu dạng hình học của HCl là tuyến tính, với góc liên kết là 180°.
 0
0
Nếu bạn muốn hỏi bài tập
Các câu hỏi của bạn luôn được giải đáp dưới 10 phút
CÂU HỎI LIÊN QUAN
Top thành viên trả lời



