Tất cả
Hỏi bài tập Toán Học
Vật Lý
Hóa Học
Tiếng Anh
Ngữ Văn
Hỏi đời sống Tâm lý cảm xúc
Tình cảm
Gia đình bạn bè
Cơ thể & Dậy thì
Giải trí
Mạng xã hội
Định hướng cuộc sống
Hỏi đáp ẩn danh
15/11/2024
một xi lanh thẳng đứng ,tiết diện S chứ k khí ở nhiệt độ 17 độ C .Pit tông đặt cách đáy xilanh một đoạn h=40 cm.Khi không khí trong xi lanh được nung đến 47 độ C thì pit tông đượcnâng lên một khoảng bằ...
 0
0
-
Câu trả lời phải chính xác, đầy đủ dựa trên kiến thức xác thực:
- ✔ Đối với câu hỏi trắc nghiệm: Đưa đáp án lựa chọn + giải thích lý do chọn đáp án.
- ✔ Đối với câu hỏi tự luận: Đưa lời giải và đáp án cho câu hỏi.
- ✔ Đối với câu hỏi trả lời ngắn: Đưa ra đáp án + giải thích lý do.
- ✔ Chấp nhận sử dụng ảnh do thành viên viết tay, ảnh cần rõ nét, không bị mờ, vỡ ảnh.
- Sử dụng ngôn ngữ rõ ràng, dễ hiểu.
- Tránh đưa ra các ý kiến cá nhân mang tính chất chủ quan.
- Nếu sử dụng thông tin từ nguồn khác, phải trích dẫn nguồn đầy đủ và chính xác.
- Tuyệt đối không được sao chép các thông tin từ các trang khác, từ AI hoặc chatGPT.



15/11/2024
 1
1
04/09/2025
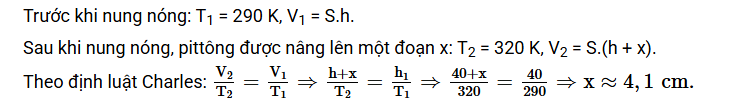
 0
0
15/11/2024
Để giải quyết vấn đề này, chúng ta cần sử dụng quy tắc khí lý tưởng. Theo quy tắc khí lý tưởng, áp suất của một khí tỷ lệ thuận với nhiệt độ của nó (được đo bằng Kelvin) khi thể tích và số mol khí giữ nguyên.
Đầu tiên, chúng ta cần chuyển nhiệt độ từ độ Celsius sang Kelvin bằng cách cộng thêm 273.15. Vì vậy, nhiệt đầu của không khí trong xi lanh là 17 độ C tương đương với 290.15 K, và nhiệt độ sau khi nung nóng là 47 độ C 320.15 K.
Theo quy tắc khí lý tưởng, áp suất của không khí trong xi lanh sẽ tăng lên theo tỷ lệ nhiệt độ tăng lên. Tỷ lệ này được tính bằng cách chia nhiệt độ sau khi nung nóng cho nhiệt độ ban đầu, tức là $\frac{320.15}{290.15} \approx 1.1$.
Điều này có nghĩa là áp suất của không khí trong xi lanh sẽ tăng lên 1.1 lần sau khi nung nóng. Vì áp suất tỷ lệ thuận với nhiệt độ, nên áp suất ban đầu của không khí trong xi lanh là P1 và áp suất sau khi nung nóng là P2, ta có:
$\frac{P2}{P1} = 1.1$
Từ đó, ta có thể tính được P2 = 1.1 * P1.
Khi pitông được nâng lên một khoảng bằng với sự tăng áp suất, nên sự tăng này sẽ được phản ánh trong của pitông. Nếu ta gọi sự tăng chiều cao của pitông là $\Delta h$, thì ta có:
$\Delta h = h * \frac{P2 - P1}{P1}$
Thay các giá trị đã biết vào công thức trên, ta có:
$\Delta h = 40 * \frac{1.1 * P1 - P1}{P1} = 40 * 0.1 = 4$
Vậy, pitông được nâng lên một khoảng bằng 4 cm.
 1
1
15/11/2024

 0
0
15/11/2024
 0
0
Nếu bạn muốn hỏi bài tập
Các câu hỏi của bạn luôn được giải đáp dưới 10 phút
CÂU HỎI LIÊN QUAN
Top thành viên trả lời



