Tất cả
Hỏi bài tập Toán Học
Vật Lý
Hóa Học
Tiếng Anh
Ngữ Văn
Hỏi đời sống Tâm lý cảm xúc
Tình cảm
Gia đình bạn bè
Cơ thể & Dậy thì
Giải trí
Mạng xã hội
Định hướng cuộc sống
Hỏi đáp ẩn danh
Nguyễn Quang Tâm
03/01/2026
Câu trong ảnh làm như nào các bạn ơi...

 0
0
Trả lời câu hỏi của Nguyễn Quang Tâm
-
Câu trả lời phải chính xác, đầy đủ dựa trên kiến thức xác thực:
- ✔ Đối với câu hỏi trắc nghiệm: Đưa đáp án lựa chọn + giải thích lý do chọn đáp án.
- ✔ Đối với câu hỏi tự luận: Đưa lời giải và đáp án cho câu hỏi.
- ✔ Đối với câu hỏi trả lời ngắn: Đưa ra đáp án + giải thích lý do.
- ✔ Chấp nhận sử dụng ảnh do thành viên viết tay, ảnh cần rõ nét, không bị mờ, vỡ ảnh.
- Sử dụng ngôn ngữ rõ ràng, dễ hiểu.
- Tránh đưa ra các ý kiến cá nhân mang tính chất chủ quan.
- Nếu sử dụng thông tin từ nguồn khác, phải trích dẫn nguồn đầy đủ và chính xác.
- Tuyệt đối không được sao chép các thông tin từ các trang khác, từ AI hoặc chatGPT.
CÂU TRẢ LỜI



Timi
03/01/2026
Trợ lý học tập AI - Câu trả lời này chỉ mang tính tham khảo
Để giải quyết các bài toán trên, ta sẽ áp dụng các phương trình hóa học và các công thức tính toán cần thiết. Dưới đây là hướng dẫn giải cho từng bài:
### Bài 1:
**Phản ứng:**
\[ 2Al + 3H_2SO_4 \rightarrow Al_2(SO_4)_3 + 3H_2 \]
**Tính số mol Al2(SO4)3:**
Khối lượng mol của Al2(SO4)3 = 2*27 + 3*(32 + 4*16) = 342 g/mol.
Số mol Al2(SO4)3:
\[
n_{Al_2(SO_4)_3} = \frac{17.1}{342} \approx 0.05 \text{ mol}
\]
**Tính số mol Al:**
Theo phản ứng, 1 mol Al2(SO4)3 cần 2 mol Al:
\[
n_{Al} = 2 * n_{Al_2(SO_4)_3} = 2 * 0.05 = 0.1 \text{ mol}
\]
Khối lượng Al:
\[
m_{Al} = n_{Al} * 27 \approx 0.1 * 27 = 2.7 \text{ g}
\]
**Tính số mol H2:**
Theo phản ứng, 1 mol Al2(SO4)3 tạo ra 3 mol H2:
\[
n_{H_2} = 3 * n_{Al_2(SO_4)_3} = 3 * 0.05 = 0.15 \text{ mol}
\]
**Tính thể tích H2:**
Sử dụng phương trình khí lý tưởng:
\[
V = nRT/P \approx n \cdot 22.4 \text{ (ở điều kiện chuẩn)} = 0.15 \cdot 22.4 \approx 3.36 \text{ lít}
\]
**Tính khối lượng dung dịch H2SO4:**
Khối lượng H2SO4 trong 20% dung dịch là:
\[
m_{H_2SO_4} = \frac{20}{100} \cdot m_{dung dịch}
\]
Tính số mol H2SO4:
\[
n_{H_2SO_4} = \frac{3}{2} * n_{Al} = \frac{3}{2} * 0.1 = 0.15 \text{ mol}
\]
Khối lượng H2SO4 cần thiết:
\[
m_{H_2SO_4} = n_{H_2SO_4} * 98 \approx 0.15 * 98 = 14.7 \text{ g}
\]
Khối lượng dung dịch:
\[
m_{dung dịch} = \frac{m_{H_2SO_4}}{0.2} \approx \frac{14.7}{0.2} = 73.5 \text{ g}
\]
### Bài 2:
**Phản ứng:**
\[ Mg + 2HCl \rightarrow MgCl_2 + H_2 \]
**Tính số mol Mg:**
\[
n_{Mg} = \frac{3.6}{24} = 0.15 \text{ mol}
\]
**Tính số mol H2:**
\[
n_{H_2} = n_{Mg} = 0.15 \text{ mol}
\]
**Tính thể tích H2:**
\[
V = 0.15 \cdot 22.4 \approx 3.36 \text{ lít}
\]
**Tính khối lượng dung dịch HCl:**
Khối lượng HCl cần thiết:
\[
n_{HCl} = 2 \cdot n_{Mg} = 2 \cdot 0.15 = 0.3 \text{ mol}
\]
Khối lượng HCl:
\[
m_{HCl} = 0.3 \cdot 36.5 = 10.95 \text{ g}
\]
Khối lượng dung dịch HCl:
\[
m_{dung dịch} = 120 \text{ g}
\]
Nồng độ % HCl:
\[
C_{HCl} = \frac{10.95}{120} \cdot 100 \approx 9.125 \%
\]
### Bài 3:
**Phản ứng:**
\[ 2Al + 3H_2SO_4 \rightarrow Al_2(SO_4)_3 + 3H_2 \]
**Tính số mol Al:**
\[
n_{Al} = \frac{1.08}{27} = 0.04 \text{ mol}
\]
**Tính số mol H2:**
\[
n_{H_2} = \frac{3}{2} \cdot n_{Al} = 0.06 \text{ mol}
\]
**Tính thể tích H2:**
\[
V = n \cdot 22.4 \approx 0.06 \cdot 22.4 \approx 1.344 \text{ lít}
\]
**Tính nồng độ dung dịch H2SO4:**
Tính số mol H2SO4:
\[
n_{H_2SO_4} = \frac{3}{2} \cdot n_{Al} = 0.06 \text{ mol}
\]
Khối lượng H2SO4:
\[
m_{H_2SO_4} = n_{H_2SO_4} \cdot 98 = 0.06 \cdot 98 = 5.88 \text{ g}
\]
Thể tích dung dịch:
\[
C = \frac{5.88}{0.4 \cdot V} \Rightarrow V = 0.4 \text{ lít}
\]
### Bài 4:
**Phản ứng:**
\[ Mg + 2HCl \rightarrow MgCl_2 + H_2 \]
**Tính số mol Mg:**
\[
n_{Mg} = \frac{0.96}{24} = 0.04 \text{ mol}
\]
**Tính số mol H2:**
\[
n_{H_2} = n_{Mg} = 0.04 \text{ mol}
\]
**Tính thể tích H2:**
\[
V = n \cdot 22.4 \approx 0.04 \cdot 22.4 \approx 0.896 \text{ lít}
\]
**Tính khối lượng dung dịch HCl:**
\[
n_{HCl} = 2 \cdot n_{Mg} = 0.08 \text{ mol}
\]
Khối lượng HCl:
\[
m_{HCl} = 0.08 \cdot 36.5 = 2.92 \text{ g}
\]
Khối lượng dung dịch:
\[
m_{dung dịch} = 200 \text{ g}
\]
Nồng độ mol HCl:
\[
C_{HCl} = \frac{0.08}{0.2} = 0.4 \text{ mol/L}
\]
### Bài 5:
**Phản ứng:**
\[ Mg + 2HCl \rightarrow MgCl_2 + H_2 \]
**Tính số mol Mg:**
\[
n_{Mg} = \frac{0.48}{24} = 0.02 \text{ mol}
\]
**Tính số mol H2:**
\[
n_{H_2} = n_{Mg} = 0.02 \text{ mol}
\]
**Tính thể tích H2:**
\[
V = n \cdot 22.4 \approx 0.02 \cdot 22.4 \approx 0.448 \text{ lít}
\]
**Tính khối lượng dung dịch HCl:**
Khối lượng HCl:
\[
m_{HCl} = 0.02 \cdot 36.5 = 0.73 \text{ g}
\]
Khối lượng dung dịch:
\[
m_{dung dịch} = 120 \text{ g}
\]
Nồng độ % HCl:
\[
C_{HCl} = \frac{0.73}{120} \cdot 100 \approx 0.6083 \%
\]
### Bài 6:
**Phản ứng:**
\[ Mg + 2HCl \rightarrow MgCl_2 + H_2 \]
**Tính số mol Mg:**
\[
n_{Mg} = \frac{0.72}{24} = 0.03 \text{ mol}
\]
**Tính số mol H2:**
\[
n_{H_2} = n_{Mg} = 0.03 \text{ mol}
\]
**Tính thể tích H2:**
\[
V = n \cdot 22.4 \approx 0.03 \cdot 22.4 \approx 0.672 \text{ lít}
\]
**Tính khối lượng dung dịch HCl:**
Khối lượng HCl:
\[
m_{HCl} = 0.03 \cdot 36.5 = 1.095 \text{ g}
\]
Khối lượng dung dịch:
\[
m_{dung dịch} = 80 \text{ g}
\]
Nồng độ mol HCl:
\[
C_{HCl} = \frac{0.03}{0.08} = 0.375 \text{ mol/L}
\]
Tóm tắt các kết quả:
- **Bài 1:** \( V \approx 3.36 \text{ lít}, m_{dung dịch} \approx 73.5 \text{ g} \)
- **Bài 2:** \( V \approx 3.36 \text{ lít}, nồng độ \approx 9.125 \% \)
- **Bài 3:** \( V \approx 1.344 \text{ lít}, m_1 \approx 0.48 \text{ g} \)
- **Bài 4:** \( m \approx 2.92 \text{ g}, V \approx 0.896 \text{ lít}, nồng độ \approx 0.4 \text{ mol/L} \)
- **Bài 5:** \( m \approx 0.73 \text{ g}, V \approx 0.448 \text{ lít}, nồng độ \approx 0.6083 \% \)
- **Bài 6:** \( m \approx 1.095 \text{ g}, V \approx 0.672 \text{ lít}, nồng độ \approx 0.375 \text{ mol/L} \)
Nếu có bất kỳ câu hỏi nào thêm, hãy cho tôi biết!
Hãy giúp mọi người biết câu trả lời này thế nào?
0/5 (0 đánh giá)
 0
0
0 bình luận
Bình luận
Minhphuong111
03/01/2026
Bài 1:
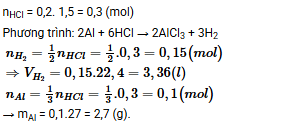
Hãy giúp mọi người biết câu trả lời này thế nào?
0/5 (0 đánh giá)
 0
0
0 bình luận
Bình luận
Nếu bạn muốn hỏi bài tập
Các câu hỏi của bạn luôn được giải đáp dưới 10 phút
CÂU HỎI LIÊN QUAN
Nguyễn Quang Tâm
06/01/2026
Nguyễn Quang Tâm
06/01/2026
Nguyễn Quang Tâm
06/01/2026
Nguyễn Quang Tâm
06/01/2026
Top thành viên trả lời
Chọn thời gian
✧˖°. 사랑🅽🅷í🅼~🅳🅰🆈🆈𝜗𝜚 ⊹ 2.210 Điểm
Nhân Irving 1.330 Điểm
Mì 2 Tôm 1.120 Điểm
Brother 1.110 Điểm
phankhoinguyen 1.100 Điểm
FQA.vn Nền tảng kết nối cộng đồng hỗ trợ giải bài tập học sinh trong khối K12. Sản phẩm được phát triển bởi CÔNG TY TNHH CÔNG NGHỆ GIA ĐÌNH (FTECH CO., LTD)
Điện thoại: 1900636019
Email: info@fqa.vn
 Địa chỉ: Số 21 Ngõ Giếng, Phố Đông Các, Phường Đống Đa, Thành phố Hà Nội, Việt Nam.
Địa chỉ: Số 21 Ngõ Giếng, Phố Đông Các, Phường Đống Đa, Thành phố Hà Nội, Việt Nam.
Người chịu trách nhiệm quản lý nội dung: Đào Trường Giang
Giấy phép thiết lập MXH số 07/GP-BTTTT do Bộ Thông tin và Truyền thông cấp ngày 05/01/2024
Copyright © 2023 fqa.vn All Rights Reserved



